トランスサイレチン(TTR)は、甲状腺ホルモン(サイロキシン)やビタミンAの輸送を担い、かつ神経の保護、記憶や認知機能維持、脳虚血からの保護といった役割をもつ、人体に重要なタンパク質です1,2)。
また、血中TTRレベルは、ATTR-CM(トランスサイレチン型心アミロイドーシス)等の疾患における予後バイオマーカーとしても有用と考えられています3)。血中TTRレベルと予後について検討した臨床試験や研究結果をご紹介します。
- 1)Liz MA, et al. Neurol Ther. 2020; 9(2): 395-402.
- 2)Vieira M, Saraiva MJ. Biomol Concepts. 2014; 5(1): 45-54.
- 3)Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
1. 血中TTRレベルと予後の関係
1)有効性の曝露-反応(E-R)解析による血清TTRレベルの影響[臨床試験]
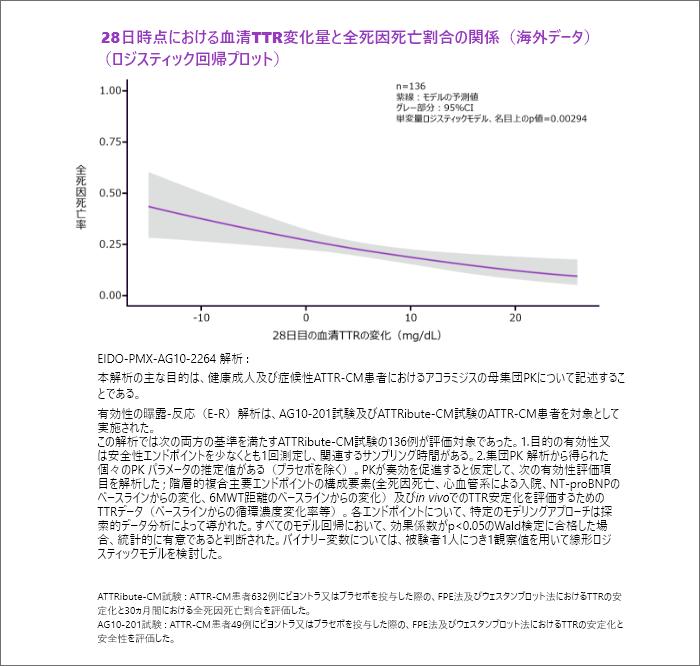
血清TTRレベルが5mg/dL増加するごとに、全死因死亡のオッズが30.6%減少すると予測されました1)。
- ATTRibute-CM試験(ビヨントラ®の海外第III相試験)と海外第II相試験のデータを使用し、TTRレベルに関する曝露-反応(E-R)解析(EIDO-PMX-AG10-2264)が実施されました。
- 治療開始28日時点*1の血清TTRレベルの増加と全死因死亡リスクの低下は関連しており、血清TTRレベルが5mg/dL増加するごとに、全死因死亡のオッズが30.6%減少すると予測されました(名⽬上のp値=0.00294、単変量ロジスティックモデル、海外データ)。
- *1:28日時点のデータはATTRibute-CM試験のみ
2)血漿TTRレベルと心不全発症リスク[疫学研究]
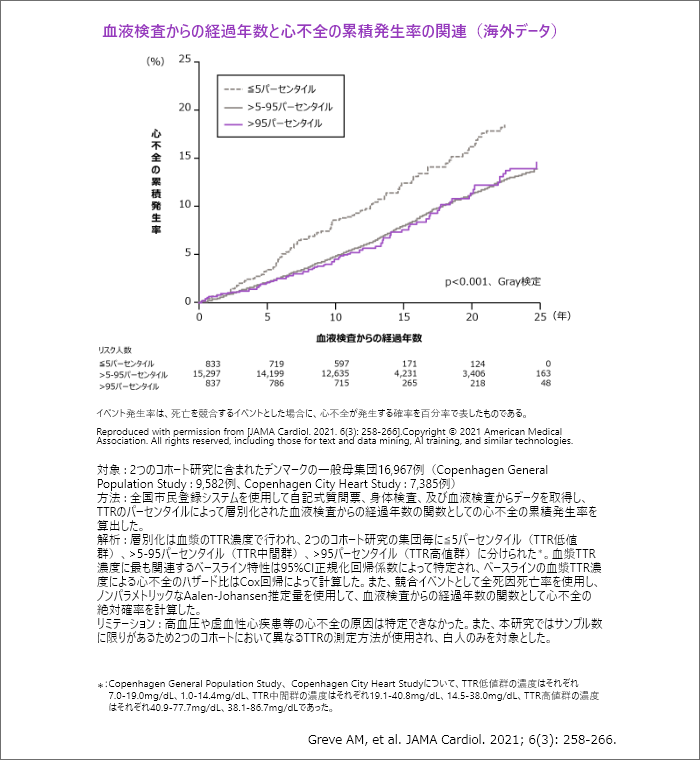
血漿TTRレベルと心不全発症との関連を検討した研究で、血漿TTR 低値群*2、中間群*2、高値群*2で比較したところ、低値群では他2群より心不全の発症リスクが有意に高いことが報告されました(p<0.001、Gray検定、海外データ)2)。
- *2:血漿TTRレベルが5パーセンタイル以下を低値群、5~95パーセンタイルを中間群、95パーセンタイル以上を高値群と定義している。
3)血清TTRレベルと死亡リスク[疫学研究]
ATTRwt-CM(野生型ATTR-CM)患者の血清TTRレベルと生存率との関連について、血清TTRを低値群*3、高値群*3で比較した研究では、血清TTR低値群は高値群と比較し生存期間が短かったことが報告されました(HR:2.3、95%CI:1.2~4.2、p=0.03、log-rank検定、海外データ)3)。
-
*3:血清TTR18mg/dLを閾値として、18mg/dL以上を高値群、18mg/dL未満を低値群と定義している。

- 1)社内資料:臨床薬理の概要(承認時評価資料)
- 2)Greve AM, et al. JAMA Cardiol. 2021; 6(3): 258-266.
- 3)Hanson JLS, et al. Circ Heart Fail. 2018; 11(2): e004000.
2. TTR不安定化がATTR-CMの発症機序
加齢や遺伝子変異によってTTR四量体が不安定化することが、ATTR-CM発症の根本原因です1,2)。
TTRは通常、四量体を形成していますが、構造の不安定化により、単量体へ解離します。単量体はミスフォールディングを起こし、集合・凝集してアミロイドを形成します2)。ATTR-CMでは、アミロイドが心臓のあらゆる構造に浸潤し3)、心臓壁の肥厚や拡張障害・収縮障害・伝導障害等を引き起こします4)。
TTRが不安定化する要因によりATTR-CMは2つのサブタイプ(野生型、遺伝性)にわけられ、それぞれ異なった特徴を有しています。2つのサブタイプはそれぞれ、加齢による変化(野生型)やTTR遺伝子の変異(変異型)等により、TTR四量体を不安定化する構造変化を引き起こす可能性があります1)。
![ATTR-CM発症の流れKittleson MM, et al. Circulation. 2020; 142(1): e7-e22. [COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]Ruberg FL, et al. J Am Coll Cardiol. 2019; 73(22): 2872-2891.[COI:著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]](/-/media/beyonttra_jp/ttr/group9000_04-img.png?rev=-1&la=ja-JP&h=345&w=700&hash=BB7F6991E06929A97784BE8BEFC209B6)
- 1)Kittleson MM, et al. Circulation. 2020; 142(1): e7-e22.
- [COI︓著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
- 2)Ruberg FL, et al. J Am Coll Cardiol. 2019; 73(22): 2872-2891.
- [COI︓著者のなかにはEidos Therapeutics, Inc. よりコンサルティング料等を受領している者やEidos Therapeutics, Inc. による臨床試験の関係者が含まれる]
- 3)Yilmaz A, et al. Clin Res Cardiol. 2021; 110(4): 479-506.
- 4)日本循環器学会(編). 2020年版心アミロイドーシス診療ガイドライン. P.9.
- https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2020_Kitaoka.pdf(2025年1月参照)
3. TTRの生体内における重要な役割
プレアルブミンとして知られるTTRは、生体内で重要な役割を担うタンパク質です1,2)。
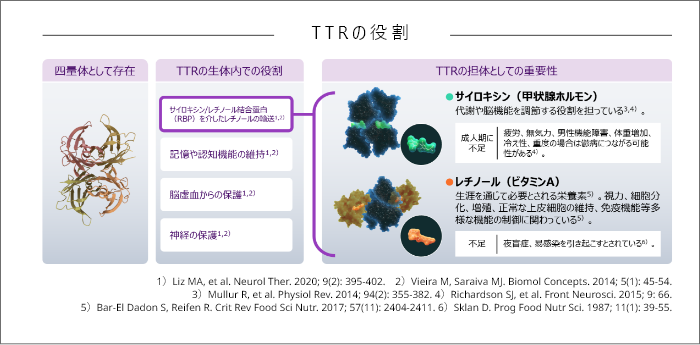
主な役割として、甲状腺ホルモンであるサイロキシン(=チロキシン)やビタミンAであるレチノールと結合したレチノール結合タンパク質(RBP)の輸送が知られ、加えてTTR自身は神経の保護、記憶や認知機能維持、脳虚血からの保護等が報告されています1,2)。TTRの大部分は、肝臓で産生され、血液中を循環します7)。また、脈絡叢や網膜色素上皮でもTTRの産生が確認されています8)。
TTRは四量体を形成しますが、二量体、単量体への解離も常に起きています9)。その平衡状態の中、TTRとしての役割を果たすのは四量体であり、輸送するサイロキシンやRBPも、四量体と結合することで脳脊髄液や血液へ輸送されます1)。TTRの半減期は約2~3日とされています10)。
TTRに輸送されるサイロキシン及びレチノールは、いずれも体内で重要な役割を持っています。
サイロキシンは、代謝3)や脳機能の調節をする役割を担っています。成人期に不足すると、疲労、無気力、男性機能障害、体重増加、冷え性、重度の場合は鬱病につながる可能性があるとされています4)。
レチノールは、生涯を通じて必要とされる栄養素で、視力、細胞分化、増殖、正常な上皮細胞の維持、免疫機能等の多様な機能の制御に関わっています5)。不足すると、夜盲症、易感染を引き起こすとされています6)。
- 1)Liz MA, et al. Neurol Ther. 2020; 9(2): 395-402.
- 2)Vieira M, Saraiva MJ. Biomol Concepts. 2014; 5(1): 45-54.
- 3)Mullur Rashmi, et al. Physiol Rev. 2014; 94(2): 355-382.
- 4)Richardson SJ, et al. Front Neurosci. 2015; 9: 66.
- 5)Bar-El Dadon S, Reifen R. Crit Rev Food Sci Nutr. 2017; 57(11): 2404-2411.
- 6)Sklan D. Prog Food Nutr Sci. 1987; 11(1): 39-55.
- 7)Hawkins PN, et al. Ann Med. 2015; 47(8): 625-638.
- 8)Ruberg FL, et al. Circulation. 2012; 126(10): 1286-1300.
- 9)横山武司 他. ⽇本中性⼦科学会誌 波紋. 2013; 23(2): 142-145.
- 10)Socolow EL, et al. J Clin Invest. 1965; 44(10): 1600-1609.







